Una de las candidatas a vacuna contra el coronavirus desarrollada por Pfizer y BioNTech, diferente a la que se comenzó a probar en la Argentina esta semana, demostró generar una "robusta" respuesta inmunológica en un ensayo clínico preliminar realizado con 45 adultos, según publicó hoy la revista Nature.
Coronavirus: otra vacuna despierta esperanza tras una "robusta" respuesta inmunológica (pero con efectos secundarios)
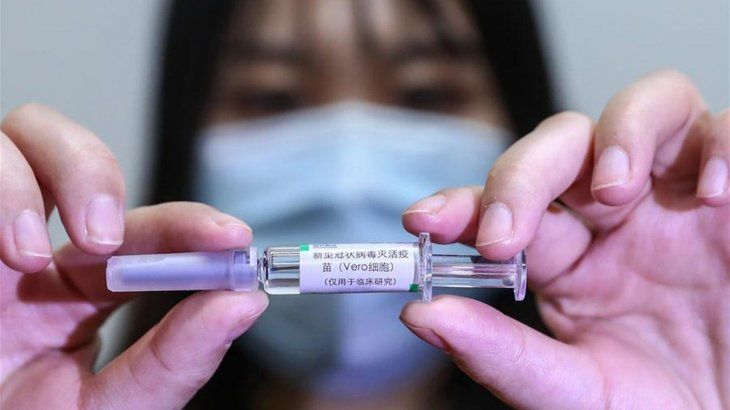
Se trata de la vacuna BNT162b1, que utiliza un ARN mensajero, esto es, una parte del virus (proteína) para generar la respuesta inmunitaria del organismo.
-
PAMI comenzó con la campaña de la vacuna antigripal 2026
-
Temporal devastador en Tucumán: familias atrapadas por el agua piden auxilio urgente tras el desborde de ríos

Desde el Ministerio de Salud buscan 10 mil voluntarios para colaborar en la vacunación contra la Covid-19.
Se trata de la vacuna BNT162b1, que utiliza un ARN mensajero, esto es, una parte del virus (proteína) para generar la respuesta inmunitaria del organismo.
Según los datos provisionales del estudio clínico en fase 1/2, realizado para evaluar la seguridad, tolerabilidad e inmunogenicidad de la vacuna, la BNT162b1, que se administra por vía intramuscular, se testó en 45 adultos sanos de 18 a 55 años de edad (23 hombres y 22 mujeres no embarazadas; 37 participantes eran de raza blanca).
Los candidatos -asignados al azar- recibieron una dosis de 10 microgramos (μg), 30 μg, 100 μg o un placebo; además, los participantes de los grupos 10μg y 30μg también recibieron una segunda dosis el día 21.
Los autores constataron que la vacuna era bien tolerada, aunque algunos participantes experimentaron en los siete días siguientes a la vacunación efectos secundarios de leves a moderados, que aumentaron con el nivel de la dosis, indicó la agencia de noticias EFE.
Las reacciones adversas más frecuentes fueron dolor local en el lugar de la inyección, fatiga, dolor de cabeza y muscular, escalofríos, fiebre y trastornos del sueño.
No obstante, la vacuna provocó una respuesta inmunológica robusta en los participantes, que aumentó con el nivel de la dosis y con una segunda dosis.
Los anticuerpos contra el SARS-CoV-2 permanecían 21 días después de la primera vacunación en todos los niveles de dosis, y se registró un aumento sustancial de los anticuerpos neutralizantes contra el virus siete días después de que se administrara la segunda dosis de 10-μg o 30-μg.
La respuesta inmunológica fue mucho más fuerte en el grupo 30-μg que en el grupo 10-μg, según se indicó en la publicación.
Sin embargo, no hubo diferencias notables en la respuesta inmunológica entre los grupos de 30-μg y 100-μg tras la primera dosis, y como los participantes que recibieron la dosis de 100-μg también experimentaron mayores efectos secundarios, no recibieron una segunda inoculación.
Los niveles de anticuerpos neutralizantes de quienes participaron fueron de 1,9 a 4,6 veces más altos que los de los pacientes que se recuperaban de la infección por el SARS-CoV-2.
Consultado sobre si se trata de la misma vacuna que se está probando en Argentina en Fase 3, cuyo proceso comenzó el lunes pasado en el Hospital Militar, Fernando Polack, el investigador a cargo del estudio que se realiza en el país, explicó que "se trata de otra de las vacunas de Pfizer".
"La que salió en el estudio publicado hoy en Nature mira la respuesta a una pequeña región de la proteína espiga (que es la que utiliza el virus para 'pegarse' a las céulas humanas), mientras que la que se está probando aquí mira la respuesta a la espiga entera", detalló.
Y continuó: "Todo indica que la respuesta a la espiga entera genera muchas menos molestias (fiebre, dolor muscular, cefale) que la respuesta del organismo a la región de la proteína que se publica en este estudio que salió hoy en Nature".
- Temas
- Vacuna
- Coronavirus











Dejá tu comentario