Washington - Nueve directores de empresas que desarrollan vacunas contra el covid-19 firmaron un compromiso de respetar el máximo rigor científico, una respuesta implícita a las preocupaciones surgidas en Estados Unidos por la aparente presión del presidente, Donald Trump, para que al menos una de ellas se dé por aprobada y comience a distribuirse antes de la elección del 3 de noviembre.
Laboratorios salen al cruce de las dudas que causa Trump y dan garantías sobre sus desarrollos
-
Artemis II explorará la cara oculta de la Luna y perderá contacto con la Tierra por un tiempo
-
Murió el jefe de inteligencia de la Guardia Revolucionaria iraní en un ataque de EEUU e Israel
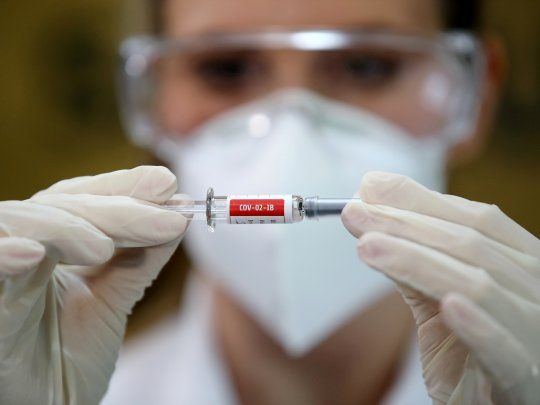
EXPECTATIVA. La atención internacional está centrada en las pruebas clínicas de diferentes vacunas contra el covid-19, único camino para ponerle fin a una pandemia que ha provocado un drama humanitario y económico.
“Nosotros, las compañías biofarmacéuticas abajo firmantes, deseamos reiterar nuestro compromiso continuo de desarrollar y probar vacunas potenciales contra el covid-19 de acuerdo con altos estándares éticos y principios científicos rigurosos”, dijeron en un comunicado conjunto, difundido ayer, los directores ejecutivos de los gigantes AstraZeneca, BioNTech, GlaxoSmithKline, Johnson & Johnson, Merck Sharp & Dohme, Moderna, Novavax, Pfizer y Sanofi.
Estas compañías se comprometieron a “presentar solo una solicitud de autorización, o v de emergencia, después de haber demostrado la seguridad y eficacia de la vacuna en el contexto de un ensayo clínico de fase 3 diseñado y realizado con el fin de cumplir con las condiciones establecidas por las autoridades reguladoras como la FDA” (la Administración de Alimentos y Medicamentos de Estados Unidos.
Precisamente sobre la FDA se centran las preocupaciones de varios expertos y exfuncionarios de salud de ese país, después de que la entidad haya autorizado para uso de emergencia, a pesar de la falta de evidencia rigurosa, dos tratamientos contra el covid-19: la hidroxicloroquina (posteriormente revocada por su falta de eficacia y sus posibles efectos adversos) y el plasma sanguíneo de pacientes recuperados, ambos promocionados por Trump.
El Centro de Control de Enfermedades (CDC) instruyó la semana pasada a los estados a preparar los procedimientos de distribución para los primeros días de noviembre, alentando la expectativa de que al menos una vacuna podría ser aprobada para entonces. La iniciativa fue considerada por muchos fruto de la presión del mandatario, rezagado en las encuestas de intención de voto y necesitado de dar un golpe de efecto que facilite su reelección.
En ese sentido, el candidato demócrata a la Casa Blanca, Joe Biden, acusó a Trump durante los últimos días de “socavar la confianza popular” al hablar en repetidas ocasiones sobre la posibilidad de tener una vacuna antes de las elecciones del 3 de noviembre.
La candidata demócrata a la vicepresidencia, Kamala Harris, en tanto, señaló que, dado que Trump tiene un historial de ignorar la opinión de los expertos en la pandemia, “no confiaría en él” y que solo estaría convencida de la eficacia y seguridad de la inmunización solo si alguien calificado así lo afirmara.
Tanto Estados Unidos como la Unión Europea intentan acelerar todos los ensayos para contar cuanto antes con la solución, tanto sanitaria como económica, a la pandemia. En ese apuro, surgen dudas sobre las condiciones de seguridad de largo plazo de las vacunas, razón por la cual varios de los principales laboratorios del mundo presionan por firmar acuerdos con los gobiernos que los pongan a salvo de posibles juicios en caso de que, en los próximos años, se comprueben efectos adversos imposibles de advertir en lo inmediato.
El presidente de Rusia, Vladímir Putin, ya anunció el logro de una vacuna, llamada Sputnik V, pero la impresión internacional generalizada de que se había salteado la fase 3 de ensayos clínicos en decenas de miles de voluntarios, lo llevó luego a dar garantías de su realización. Así, en paralelo a esa experimentación, el Gobierno de Moscú dijo ayer que la primera partida ya es distribuida en los centros sanitarios del país para su aplicación en grupos de riesgo como personal sanitario y docente, además de los voluntarios.
En tanto, el jefe de la FDA estadounidense garantizó un proceso puramente científico para juzgar la efectividad de una vacuna.
Comités de expertos independientes supervisan en Estados Unidos los ensayos clínicos de las vacunas de Moderna y Pfizer.
La FDA depende de estos comités independientes y de los fabricantes de vacunas, quienes deben presentar una solicitud de autorización.
Según Anthony Fauci, director del Instituto Nacional de Enfermedades Infecciosas, no se espera que los resultados de estas pruebas se conozcan hasta los últimos dos meses del año.
“Es extremadamente improbable, pero no imposible”, que haya resultados antes de las elecciones, dijo a la radio NPR el científico jefe del equipo de la Casa Blanca para la producción de vacunas, Moncef Slaoui.













Dejá tu comentario